پارکینسون
پارکینسون
راهنمای جامع بیماری پارکینسون: از علل و علائم تا تشخیص و درمان نوین
مقدمه
بیماری پارکینسون (Parkinson’s Disease) یک اختلال پیشرونده و دژنراتیو (تخریبکننده) سیستم عصبی است که با گذشت زمان تشدید میشود. سیستم عصبی شبکهای پیچیده از سلولهای عصبی است که بسیاری از بخشهای بدن، از جمله توانایی حرکت را کنترل میکند. اگرچه این بیماری بیشتر به دلیل تأثیرات آن بر کنترل عضلات، تعادل و حرکت شناخته میشود، اما میتواند طیف وسیعی از اثرات دیگر را بر حواس، توانایی تفکر، سلامت روان و عملکرد سیستم خودمختار بدن داشته باشد.
شیوع این بیماری با افزایش سن رابطه مستقیم دارد و معمولاً علائم آن در افراد بالای ۶۰ سال ظاهر میشود. پارکینسون دومین بیماری شایع دژنراتیو مغزی وابسته به سن (پس از آلزایمر) است و تخمین زده میشود که حداقل ۱ درصد از جمعیت بالای ۶۰ سال در سراسر جهان را تحت تأثیر قرار میدهد. اگرچه شروع بیماری در سنین پایینتر (حتی ۲۰ سالگی) تحت عنوان پارکینسون زودرس (Early-onset Parkinson’s) ممکن است رخ دهد، اما این موارد بسیار نادر بوده و اغلب ریشه ژنتیکی قوی دارند. مردان کمی بیشتر از زنان در معرض ابتلا به این بیماری هستند.
مکانیسم بیولوژیکی و علت بیماری پارکینسون
در بیماری پارکینسون، ناحیه خاصی از مغز به نام عقدههای قاعدهای (Basal Ganglia) دچار تخریب میشود. با از بین رفتن سلولهای این ناحیه، تواناییهایی که توسط آن کنترل میشدند نیز از دست میروند. تحقیقات نشان دادهاند که تغییرات شیمیایی عمدهای در مغز بیماران رخ میدهد.
نقش دوپامین و پیامرسانهای عصبی
در شرایط عادی، مغز از مواد شیمیایی به نام انتقالدهندههای عصبی (Neurotransmitters) برای ارتباط بین سلولهای عصبی (Neurons) استفاده میکند. یکی از حیاتیترین این مواد، دوپامین (Dopamine) است. سلولهای عصبی در ناحیهای از ساقه مغز به نام “توده سیاه” (Substantia Nigra) مسئول تولید دوپامین هستند. در بیماری پارکینسون، این سلولها به آرامی تخریب شده یا میمیرند.
زمانی که مغز سیگنالهای فعالسازی را برای حرکت عضلات ارسال میکند، از سلولهای وابسته به دوپامین برای تنظیم دقیق این حرکات استفاده میکند. کاهش سطح دوپامین منجر به فعالیت نامنظم مغز شده و باعث بروز علائم اصلی پارکینسون مانند کندی حرکت و لرزش میشود. علاوه بر دوپامین، بیماران ممکن است نورپینفرین (Norepinephrine) را نیز از دست بدهند؛ مادهای که عملکردهای غیرارادی بدن مانند فشار خون را کنترل میکند.
محققان تغییرات میکروسکوپی خاصی را در مغز بیماران پارکینسونی مشاهده کردهاند:
-
اجسام لویی (Lewy Bodies): تودههایی از پروتئینهای خاص در مغز که شاخص اصلی میکروسکوپی پارکینسون هستند.
-
آلفا-سینوکلئین (Alpha-synuclein): پروتئینی که در تمام اجسام لویی یافت میشود. در حالت بیماری، این پروتئین دچار تغییر شکل شده و به صورت تودههایی در میآید که سلول قادر به شکستن آنها نیست. تجمع این پروتئینها اثرات سمی داشته و باعث آسیب سلولی میشود.
-
تغییرات میتوکندریایی: تغییر در میتوکندریها (Mitochondria)، که موتورخانه تولید انرژی سلول هستند، نیز در مغز بیماران مشاهده شده است.

علل ژنتیکی و محیطی پارکینسون
علت دقیق بیماری هنوز ناشناخته است، اما ترکیبی از عوامل زیر نقش دارند:
-
ژنتیک: حدود ۱۰ درصد موارد منشأ خانوادگی دارند. جهشهای ژنی خاصی کشف شدهاند که با بیماری مرتبط هستند، اما در اکثر موارد، نقش ژنتیک تنها زمانی پررنگ است که چندین عضو خانواده مبتلا باشند.
-
عوامل محیطی: قرار گرفتن در معرض سموم خاص مانند علفکشها، آفتکشها و مواد صنعتی خاص (مانند MPTP یا گرد و غبار منگنز) میتواند ریسک ابتلا را افزایش دهد، هرچند هیچ عامل محیطی به تنهایی به عنوان علت قطعی اثبات نشده است.
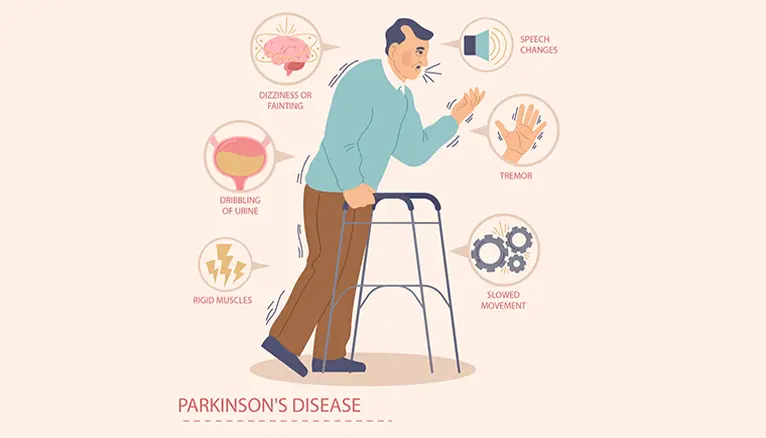
علائم و نشانههای بیماری پارکینسون
علائم پارکینسون برای هر فرد متفاوت است و اغلب به آهستگی آغاز میشوند. علائم معمولاً از یک طرف بدن شروع شده و با گذشت زمان به طرف دیگر نیز گسترش مییابند، اما معمولاً در سمت اولیه شدیدتر باقی میمانند. این علائم به دو دسته کلی تقسیم میشوند:
۱. علائم حرکتی بیماری پارکینسون
تشخیص پارکینسون عمدتاً بر اساس این علائم صورت میگیرد:
-
کندی حرکت: این علامت لازمه تشخیص بیماری است. کارهای ساده روزمره مانند برخاستن از صندلی، بستن دکمهها یا دوش گرفتن دشوار و زمانبر میشود. بیمار ممکن است احساس ضعف عضلانی کند، اما در واقع مشکل در کنترل عضله است نه قدرت آن.
-
لرزش: لرزش ریتمیک که معمولاً در حالت استراحت رخ میدهد و در حدود ۸۰ درصد بیماران دیده میشود. این لرزش اغلب در دستها یا انگشتان آغاز میشود و ممکن است به صورت حرکت “قرصپیچ” باشد (مالش انگشت شست و اشاره به هم). لرزش ممکن است در پا یا فک نیز رخ دهد و معمولاً هنگام انجام کار یا حرکت کاهش مییابد.
-
سفتی و خشکی عضلات : عضلات ممکن است در هر قسمتی از بدن سفت و دردناک شوند. دو نوع سفتی شایع است: “سفتی لوله سربی” (Lead-pipe rigidity) که سفتی مداوم است و “سفتی چرخدندهای” (Cogwheel stiffness) که ترکیبی از لرزش و سفتی است و حرکت اندام به صورت پلهپله انجام میشود.
-
مشکلات تعادل و قامت : قامت بیمار ممکن است خمیده شود. گامها کوتاه و کشیده میشوند و چرخش بدن هنگام راه رفتن دشوار میگردد. دستها هنگام راه رفتن کمتر نوسان میکنند .
-
تغییرات چهره : صورت بیمار ممکن است حالتی ماسکمانند و بدون احساس پیدا کند و پلک زدن کاهش یابد.
-
ریزنویسی : دستخط بیمار کوچک و فشرده میشود.
۲. علائم غیرحرکتی پارکینسون
شواهد نشان میدهد که این علائم ممکن است سالها یا حتی دههها قبل از علائم حرکتی ظاهر شوند و به عنوان “علائم هشداردهنده زودهنگام” عمل کنند:
-
از دست دادن حس بویایی: کاهش یا از دست دادن کامل بویایی.
-
مشکلات خواب: شامل اختلال رفتار در خواب REM (که در آن بیمار رویاهای خود را به صورت فیزیکی اجرا میکند)، سندرم پاهای بیقرار و بیدار شدنهای مکرر.
-
مشکلات خلقی و شناختی: افسردگی، اضطراب، و در مراحل پیشرفتهتر، دمانس (Dementia) یا زوال عقل و مشکلات حافظه و تمرکز.
-
اختلالات سیستم اتونومیک: شامل یبوست شدید، تکرر ادرار یا بیاختیاری، و افت فشار خون وضعیتی (Orthostatic Hypotension) که باعث سرگیجه هنگام ایستادن میشود.
-
تغییرات گفتاری: صحبت کردن با صدای آرام ، یکنواخت یا لکنتمانند.
-
مشکلات بلع : که میتواند منجر به ریزش آب دهان و خطر خفگی شود.
تفاوت پارکینسون با پارکینسونیسم (Parkinsonism)
“پارکینسونیسم” یک اصطلاح کلی است که به مجموعهای از علائم مشابه پارکینسون اشاره دارد. بیماری پارکینسون شایعترین نوع آن است، اما شرایط دیگری نیز وجود دارند که علائم مشابه ایجاد میکنند، مانند:
-
پارکینسونیسم دارویی: ناشی از مصرف برخی داروهای روانپزشکی (که معمولاً با قطع دارو قابل برگشت است).
-
آتروفی سیستم چندگانه (Multiple System Atrophy).
-
فلج فوق هستهای پیشرونده (Progressive Supranuclear Palsy).
-
پارکینسونیسم عروقی: ناشی از سکتههای مغزی کوچک متعدد.
تشخیص پارکینسون
هیچ آزمایش واحدی برای تشخیص قطعی پارکینسون وجود ندارد. تشخیص عمدتاً بالینی و بر اساس تاریخچه پزشکی و معاینه عصبی توسط متخصص مغز و اعصاب انجام میشود.
پزشکان ممکن است از معیارهای درجهبندی مانند MDS-UPDRS استفاده کنند که جنبههای حرکتی و غیرحرکتی زندگی روزمره بیمار را ارزیابی میکند.
آزمایشهای تکمیلی برای تشخیص بیماری پارکینسون:
اگرچه آزمایش خون و تصویربرداری معمولاً برای تشخیص خودِ پارکینسون کاربرد ندارند، اما برای رد کردن سایر بیماریها استفاده میشوند:
-
MRI و CT Scan: برای بررسی ساختار مغز و رد کردن تومور یا سکته.
-
PET Scan و DaTscan: میتوانند کاهش فعالیت دوپامین در مغز را نشان دهند.
-
تستهای نوین: تحقیقات جدید روشهایی مانند “بیوپسی پوست” (Skin biopsy) یا “نمونهگیری از مایع نخاعی” (Spinal tap) را برای شناسایی پروتئین آلفا-سینوکلئین تغییرشکلیافته پیشنهاد میدهند که میتواند به تشخیص دقیقتر کمک کند.
درمان و مدیریت پارکینسون
بیماری پارکینسون درمان قطعی ندارد، اما داروها و روشهای درمانی میتوانند علائم را به طور چشمگیری کنترل کنند.
۱. دارودرمانی پارکینسون
هدف داروها افزایش سطح دوپامین یا شبیهسازی اثرات آن است:
-
لوودوپا (Levodopa): مؤثرترین داروی پارکینسون است. این ماده در مغز به دوپامین تبدیل میشود. معمولاً همراه با کاربیدوپا (Carbidopa) تجویز میشود تا از تجزیه زودرس آن در بدن جلوگیری کرده و عوارضی مانند تهوع را کاهش دهد. مصرف طولانیمدت آن ممکن است اثربخشی را کم کرده یا عوارض حرکتی ایجاد کند.
-
آگونیستهای دوپامین (Dopamine Agonists): این داروها به جای جایگزینی دوپامین، رفتار آن را در مغز تقلید میکنند. معمولاً در بیماران جوانتر برای به تعویق انداختن شروع لوودوپا تجویز میشوند.
-
مهارکنندههای آنزیم (MAO-B Inhibitors و COMT Inhibitors): این داروها (مانند Selegiline یا Entacapone) با جلوگیری از تجزیه دوپامین طبیعی یا لوودوپا، به ماندگاری بیشتر آنها در مغز کمک میکنند.
-
آنتیکولینرژیکها (Anticholinergics): برای کمک به کاهش لرزش و سفتی عضلات.
-
آمانتادین (Amantadine): برای تسکین کوتاهمدت علائم خفیف و کنترل حرکات غیرارادی ناشی از مصرف لوودوپا.
۲. درمانهای جراحی پارکینسون
-
تحریک عمقی مغز (Deep Brain Stimulation – DBS): در این روش، الکترودهایی در نواحی خاصی از مغز کاشته میشوند که به یک دستگاه تولیدکننده ضربان (مشابه ضربانساز قلب) در قفسه سینه متصل هستند. پالسهای الکتریکی ملایم میتوانند علائم حرکتی شدید (مانند لرزش و سفتی) را که به دارو پاسخ نمیدهند، کنترل کنند. این روش برخلاف جراحیهای قدیمی که باعث تخریب بافت مغز میشدند، برگشتپذیر است.
۳. درمانهای حمایتی و سبک زندگی
-
فیزیوتراپی: برای بهبود تعادل، انعطافپذیری و راه رفتن.
-
گفتاردرمانی: برای بهبود مشکلات تکلم و بلع.
-
ورزش: ورزشهای هوازی، تایچی و رقص میتوانند به حفظ تعادل و تحرک کمک کنند.
-
رژیم غذایی: مصرف فیبر کافی برای جلوگیری از یبوست و نوشیدن آب زیاد. تحقیقاتی نشان دادهاند که مصرف کافئین (قهوه و چای سبز) ممکن است با ریسک کمتر ابتلا مرتبط باشد.
۴. درمانهای تجربی و آیندهنگر
تحقیقات بر روی سلولهای بنیادی برای جایگزینی نورونهای از دست رفته، ژندرمانی و درمانهای ترمیم نورون در حال انجام است که امیدهای تازهای را ایجاد کردهاند.
عوارض و پیشآگهی پارکینسون
پارکینسون به خودی خود کشنده نیست، اما عوارض ناشی از آن (مانند ذاتالریه ناشی از مشکل بلع یا صدمات ناشی از زمین خوردن) میتواند خطرناک باشد.
امید به زندگی در بیماران پارکینسون به لطف پیشرفتهای درمانی به طور قابل توجهی افزایش یافته و نزدیک به افراد عادی است. بیماری پیشرونده است و در مراحل نهایی ممکن است بیمار برای انجام کارهای روزمره به کمک کامل نیاز داشته باشد. زوال عقل و توهم نیز ممکن است در مراحل پیشرفته رخ دهد.
پیشگیری از پارکینسون
از آنجا که علت دقیق بیماری ناشناخته است، روش قطعی برای پیشگیری وجود ندارد. با این حال، برخی مطالعات نشان دادهاند که ورزش منظم هوازی و مصرف نوشیدنیهای کافئیندار ممکن است اثر محافظتی داشته باشند. همچنین برخی داروها مانند ایبوپروفن و استاتینها در برخی تحقیقات با کاهش ریسک مرتبط بودهاند، اما نیاز به شواهد بیشتری است.
روشهای درمان پارکینسون در سال ۲۰۲۵
- دارودرمانی: داروهایی مانند لوودوپا (Levodopa) رایجترین درمان برای جبران کمبود دوپامین هستند. در سال ۲۰۲۵، داروهای جدیدی مانند Tavapadon نیز در مراحل تأیید نهایی برای استفاده قرار گرفتهاند.
- جراحی DBS: تحریک عمیق مغزی (Deep Brain Stimulation) که در آن الکترودهایی در مغز کاشته میشود تا فعالیتهای غیرعادی الکتریکی را کنترل کند.
- تغییر سبک زندگی: ورزشهای هوازی منظم، فیزیوتراپی و رژیم غذایی سرشار از فیبر و ویتامینهای D و E نقش مهمی در مدیریت بیماری دارند.
نتیجهگیری
بیماری پارکینسون یک اختلال پیچیده است که فراتر از لرزش دست، بر تمامی جنبههای زندگی فرد تأثیر میگذارد. اگرچه تشخیص آن میتواند نگرانکننده باشد، اما درک دقیق از ماهیت بیماری، مکانیسمهای دوپامینرژیک و گزینههای درمانی متنوع موجود، به بیماران کمک میکند تا کیفیت زندگی خود را حفظ کنند. با مدیریت صحیح دارویی، تغییرات سبک زندگی و حمایت تیم پزشکی، اکثر بیماران میتوانند سالهای متمادی زندگی مستقل و فعالی داشته باشند. تحقیقات مداوم در زمینه بیومارکرها و درمانهای هدفمند ژنتیکی، نویدبخش آیندهای روشنتر برای مدیریت و شاید درمان قطعی این بیماری است.